ЛЕКЦИИ
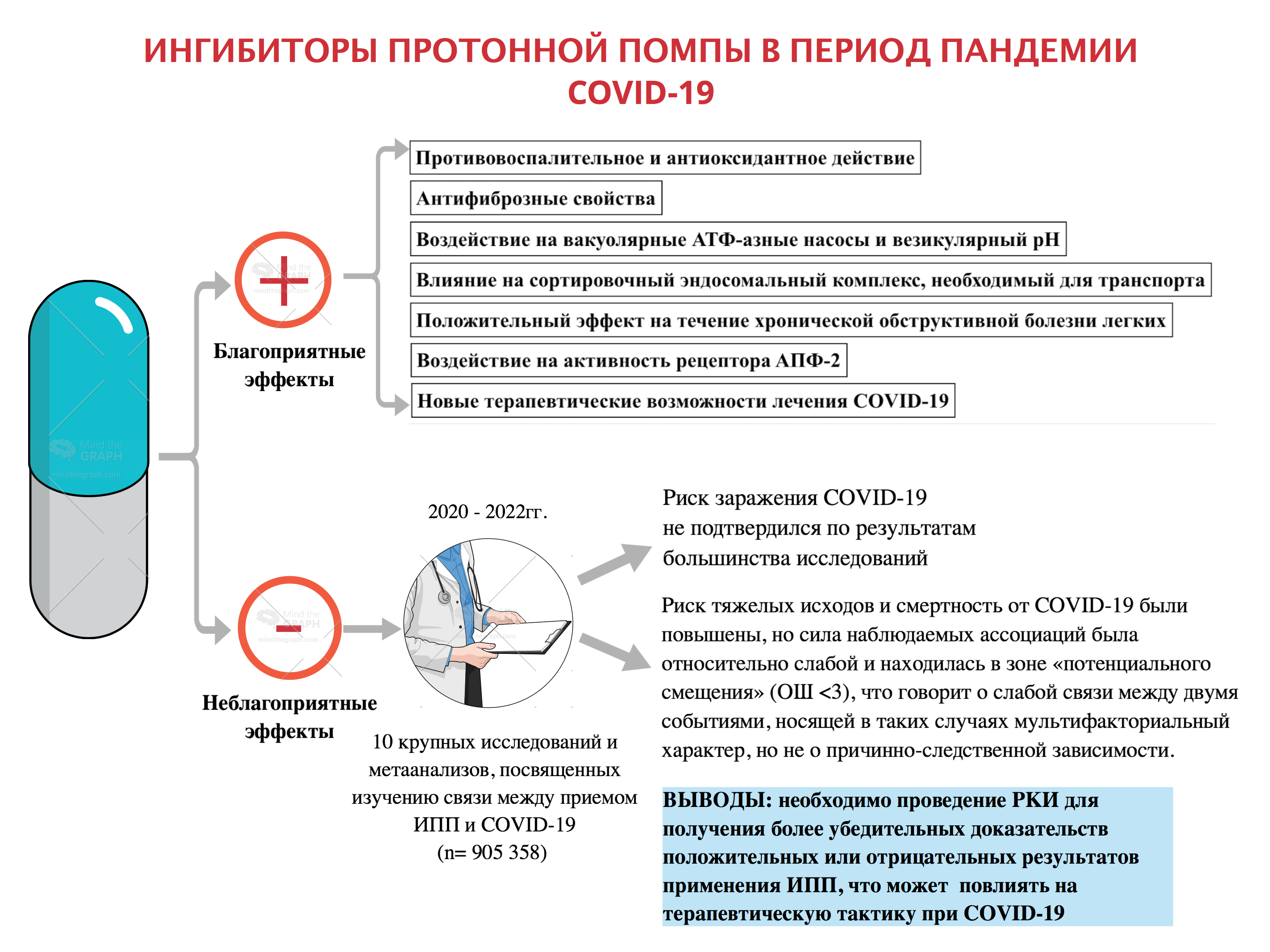
Безопасность применения ингибиторов протонной помпы (ИПП) при коронавирусной инфекции (COVID-19) является недостаточно изученной. ИПП являются мощными супрессорами желудочной секреции и входят в десятку наиболее широко используемых препаратов в мире. Предполагается, что препараты влияют на восприимчивость к вирусу, тяжесть течения и исходы у пациентов с диагнозом COVID-19. Это беспокойство основано на механизме действия ИПП — подавлении кислотности желудочного сока, который считается первой линией защиты от инфекций. В совокупности результаты большинства исследований и метаанализов подтверждают возможность того, что использование ИПП может способствовать развитию более тяжелой формы COVID-19. Однако учесть все потенциальные факторы риска тяжести COVID-19 в реальной клинической практике представляется затруднительным, поэтому следует с большой осторожностью относиться к выводам о причинно-следственных связях применения ИПП. Дополнительная интересная точка зрения на использование ИПП во время пандемии заключается в том, что их прием может привести к снижению всасывания некоторых витаминов. С другой стороны, в литературе появилось несколько исследований в отношении защитных терапевтических эффектов ИПП. Все больше доказательств иммуномодулирующей и антифиброзной роли ИПП, что может быть использовано в лечении COVID-19. Кроме того, способность препаратов подщелачивать содержимое эндосом и лизосом служит препятствием для проникновения вируса в клетки. В представленном обзоре проанализированы возможные эффекты приема ИПП у пациентов с COVID-19.
ОБЗОРНЫЕ СТАТЬИ
Остеопороз — широко распространенное метаболическое заболевание скелета среди лиц 50 лет и старше. Значимым проявлением заболевания являются ост еопоретические переломы, которые могут оказывать существенное влияние на качество жизни. Целью данной публикации является рассмотрение подходов к ведению пациентов с острым остеопоретическим переломом. Данная работа разделена на две части. В первой части рассматриваются общие сведения об остеопорозе, варианты течения остеопоретического перелома, дифференциальный диагноз болевого синдрома, методы визуализации переломов, дифференциальная диагностика остеопороза. Во второй части работы рассматриваются особенности дифференциальной диагностики остеопоретического перелома по данным визуализирующих методов, немедикаментозные, медикаментозные и хирургические методы лечения.
Идиопатический легочный фиброз (ИЛФ) является тяжелым прогрессирующим заболеванием легких неизвестной этиологии со средней распространенность ю 15 на 100000 населения в мире. Различают спорадические, синдромальные и семейные случаи болезни. Спорадические случаи относятся к многофакторным заболеваниям и ассоциированы с возрастом, вирусными инфекциями, курением и вдыханием пыли, контактом с химическими реагентами и лекарствами, гастроэзофагальной рефлюксной болезнью. Выявлена ассоциация спорадического ИЛФ с аллельными вариантами генов AKAP13, ATP11A, DPP9, DSP, IVD, IL1RN, FAM13A, MUC5B, SFTPC, SPPL2C, TERC, TERT, TOLLIP. Синдромальный ИЛФ описан при синдроме Германского-Пудлака. Семейные случаи болезни обусловлены мутациями в генах, кодирующих белки сурфактанта (SFTPC), муцина (MUC5B), нуклеазу деаденилирования (PARN), участвующие в функционировании теломер (RTEL1, TERC, TERT). В 2000 году Американское торакальное сообщество рекомендовало глюкокортикоиды и цитостатики для лечения ИЛФ с целью воздействия на воспалительный процесс при активации фибробластов и их аккумулировании во внеклеточном матриксе легких. Эти рекомендации до сих пор используются практике, несмотря на публикации достоверных данных о повышенной смертности и случаев госпитализации пациентов с ИЛФ, принимающих преднизолон и азатиоприн. Согласно данным недавних метаанализов, наиболее эффективными в лечении ИЛФ являются пирфенидон (ингибитор синтеза факторов роста проколлагенов I и II) и нинтенадиб (ингибитор тирозинкиназы). Поскольку важную роль в этиопатогенезе болезни играют генетические факторы, перспективен поиск методов таргетной терапии с использованием в качестве мишеней специфических некодирующих РНК, изменения экспрессии которых не характерны для других бронхолегочных заболеваний. К ним относятся miR-9-5p, miR-27b, miR-153, miR-184, miR-326, miR-374, miR-489, miR-630, miR-1343 (уровень их снижается при болезни); miR-340, miR-424, miR-487b, miR-493, lncRNA AP003419.16, lncRNA AP003419.16 (повышенная экспрессия при ИЛФ).
Своевременное выявление врачами общей медицинской практики психических и психосоматических расстройств у пациенток при планировании, а также во время ведения беременности и в послеродовый период, остается значимой медицинской задачей. Частота встречаемости гетерогенных психосоматических расстройств (аффективные, тревожные, дисморфические, соматовегетативные, психотические) на фоне менструаций, беременности и в послеродовом периоде достигает 80 %. В свою очередь, психосоматические расстройства являются факторами риска для отсроченного наступления и сокращения продолжительности менструаций, развития предменструального синдрома, неадекватных эмоциональных реакций при менструациях, перебоев в цикле, снижения регулярности и удовлетворенности половой жизнью, фертильности, невынашивания беременности, сокращения лактационного периода, раннего наступления менопаузы с большой длительностью и клинической тяжестью пременопаузы и др. При индивидуальном подходе к назначению схемы лечения требуется учитывать факторы риска (наследственность, коморбидные расстройства, пол, возраст и др.) развития нежелательных явлений (НЯ), баланс эффективности и безопасности лекарственных средств.
Заболеваемость язвенным колитом в последние годы растет, и его развитие в молодом возрасте стало тенденцией, которая прогностически неблагоприятна. Клиническая картина язвенного колита часто расплывчата, что приводит к изначально ошибочному диагнозу. Оценка эффективности лечения и риска рецидива язвенного колита, требующая инвазивного вмешательства — одна из основных диагностических проблем. Целью исследования был анализ данных современной научной литературы о неинвазивных биомаркерах язвенного колита. Проанализированы данные зарубежных и отечественных статей по теме исследования, опубликованных в Pubmed и eLibrary за последние 5-10 лет. Биомаркеры нейтрофильного происхождения являются перспективным направлением в первичной диагностике и оценке активности язвенного колита.
Хроническая сердечная недостаточность (ХСН) является одной из наиболее распространенных и тяжелых форм ишемической болезни сердца (ИБС), на фоне которой существенно снижается продолжительность и качество жизни пациентов. Применяемые в настоящее время фармакологические и немедикаментозные методы лечения недостаточно эффективны, а трансплантация сердца ограничена организационными и техническими сложностями, возникающими при выполнении этого оперативного вмешательства, а также недостаточной доступностью донорских органов. Известно, что потенциал клеток миокарда к репарации невелик, поэтому регенеративная терапия может быть востребована, как новое перспективное направление лечения ХСН. Существует несколько направлений клеточной терапии, способствующей улучшению процессов репарации миокарда. Одним из них является трансплантация соматических стволовых клеток, которая считается безопасной и несколько улучшает сократимость миокарда, преимущественно за счет паракринных механизмов регуляции клеточного цикла. В качестве альтернативы этой методики, для трансплантации непосредственно в поврежденные участки миокарда могут быть использованы кардиомиоциты, полученные из индуцированных плюрипотентных стволовых клеток (iPSC). Однако до начала применения таких клеток у лиц, страдающих ХСН, предстоит решить проблемы их потенциальной онкогенности и недостаточно хорошей выживаемости в условиях редукции кровотока на фоне тяжелого коронарного атеросклероза. В ряде исследований рассматривались и другие направления клеточной терапии, в частности бесклеточный подход к прямому перепрограммированию, заключавшийся в преобразовании эндогенных сердечных фибробластов в индуцированные кардиомиоцитоподобные клетки. В обзоре рассматривается текущая ситуация и перспективы использования регенеративных клеточных и бесклеточных технологий при ХСН, которые могут быть введены в клиническую практику в ближайшем будущем.
ОРИГИНАЛЬНЫЕ СТАТЬИ
Введение: данные о виде, частоте и продолжительности остаточных симптомов после COVID-19 неоднородны, что связано с методологическими особенностями проведения исследований. Цель: оценка частоты и выраженности симптомов в отдаленном периоде после перенесенной новой коронавирусной инфекции.
Материалы и методы: Проведен телефонный опрос пациентов, госпитализированных в ЛРЦ МЗ РФ в связи с COVID-19 в период 13.04.2020-10.06.2020: 195 пациентов (58,2 % выписанных) через 143 (131-154) дней после дебюта заболевания и 183 (54,6 % выписанных) через 340 (325-351) дней.
Результаты: Субъективная оценка состояния своего здоровья по 100-балльной шкале до и после перенесенного COVID-19 на первом опросе составила 95 (80-100) и 80 (70-96) баллов (p< 0,001 для сравнении оценки до и после заболевания), на втором — 90 (80-100) и 80 (60-90) баллов, (p< 0,001 для сравнении оценки до и после заболевания и для сравнения оценки состояния здоровья после COVID-19 на двух этапах опроса). Разнообразные жалобы выявлены у 63 % опрошенных на первом этапе и у 75 % — на втором, количество выявленных симптомов составило 2 (0-6) и 4 (1-8) соответственно. Наиболее частыми жалобами были слабость/утомляемость (31,3 и 47,5 % опрошенных), боли в суставах (31,3 и 47,5 %) и одышка/чувство нехватки воздуха (31,3 и 43,2 %). Рост этих показателей можно связывать с изменением методики опроса. Выраженность лидир ующих симптомов на втором опросе при оценке по десятибалльной шкале была низкой: утомляемость 3 (0-6) баллов, боль в суставах, слабость и одышка — 0 (0-5) баллов, чувство нехватки воздуха — 0(0-3) балла.
Заключение: снижение самочувствия сохраняется в течение длительного времени после перенесенной коронавирусной инфекции у значительной доли пациентов, однако выраженность лидирующих симптомов к 12 месяцу наблюдения достаточно низка.
По данным литературы аутоантитела IgA к антигену CD74 рассматриваются в качестве возможного маркера для диагностики аксиальных спондилоартритов (СпА). У пациентов с болью в спине в связи с дегенеративно-дистрофическими заболеваниями позвоночника (ДДЗП) уровень аутоантител к CD74 не изучался. Представляет интерес сопоставление уровня аутоантитела IgA к антигену CD74 у пациентов с хронической болью в спине при р азличных заболеваниях. Цель настоящего исследования — сравнение уровней аутоантитела IgA к антигену CD74 у пациентов со СпА и ДДЗП. Материалы и методы. В исследовании включено 87 пациентов (55 мужчин, средний возраст 41 [29; 49] лет) со СпА, отвечающих критериям аксиального спондилоартрита Assessment of Spondyloarthritis International Society (2009), и 39 пациентов (25 мужчин, средний возраст 45 [34; 53] лет) с ДДЗП, верифицированных неврологом (коды МКБ-Х — М 51.1 и М 54.4). Методом количественного иммуноферментного анализа измеряли содержание аутоантител IgA к CD74 в образцах сывороток у пациентов со СпА и ДДЗП. Результаты. Средний уровень аутоантител IgA к CD74 у пациентов со СпА составил 11,3 [5,4; 19,4] Ед/мл, у пациентов с ДДЗП — 6,9 [4,5; 13,7] Ед/мл (p=0,024). Концентрация аутоантитела IgA к антигену CD74, превышающая пороговое значение, выявлена у 58 (66,7 %) пациентов со СпА и только у 11 (28,2 %) пациентов с ДДЗП (p<0,001). У пациентов с ДДЗП повышение уровня аутоантител IgA к CD74 выявлено у 10 (40 %) из 25 мужчин и у 1 (7,1 %) из 14 женщин (р = 0,029, χ2 = 4,785). Выводы. У 2/3 пациентов со СпА установлено повышение уровня аутоантител IgA к CD74. При этом у пациентов со спондилоартритами значимо повышена концентрация аутоантител IgA к CD74 по сравнению с пациентами с ДДЗП. >< 0,001). У пациентов с ДДЗП повышение уровня аутоантител IgA к CD74 выявлено у 10 (40 %) из 25 мужчин и у 1 (7,1 %) из 14 женщин (р = 0,029, χ2 = 4,785). Выводы. У 2/3 пациентов со СпА установлено повышение уровня аутоантител IgA к CD74. При этом у пациентов со спондилоартритами значимо повышена концентрация аутоантител IgA к CD74 по сравнению с пациентами с ДДЗП.
РАЗБОР КЛИНИЧЕСКИХ СЛУЧАЕВ
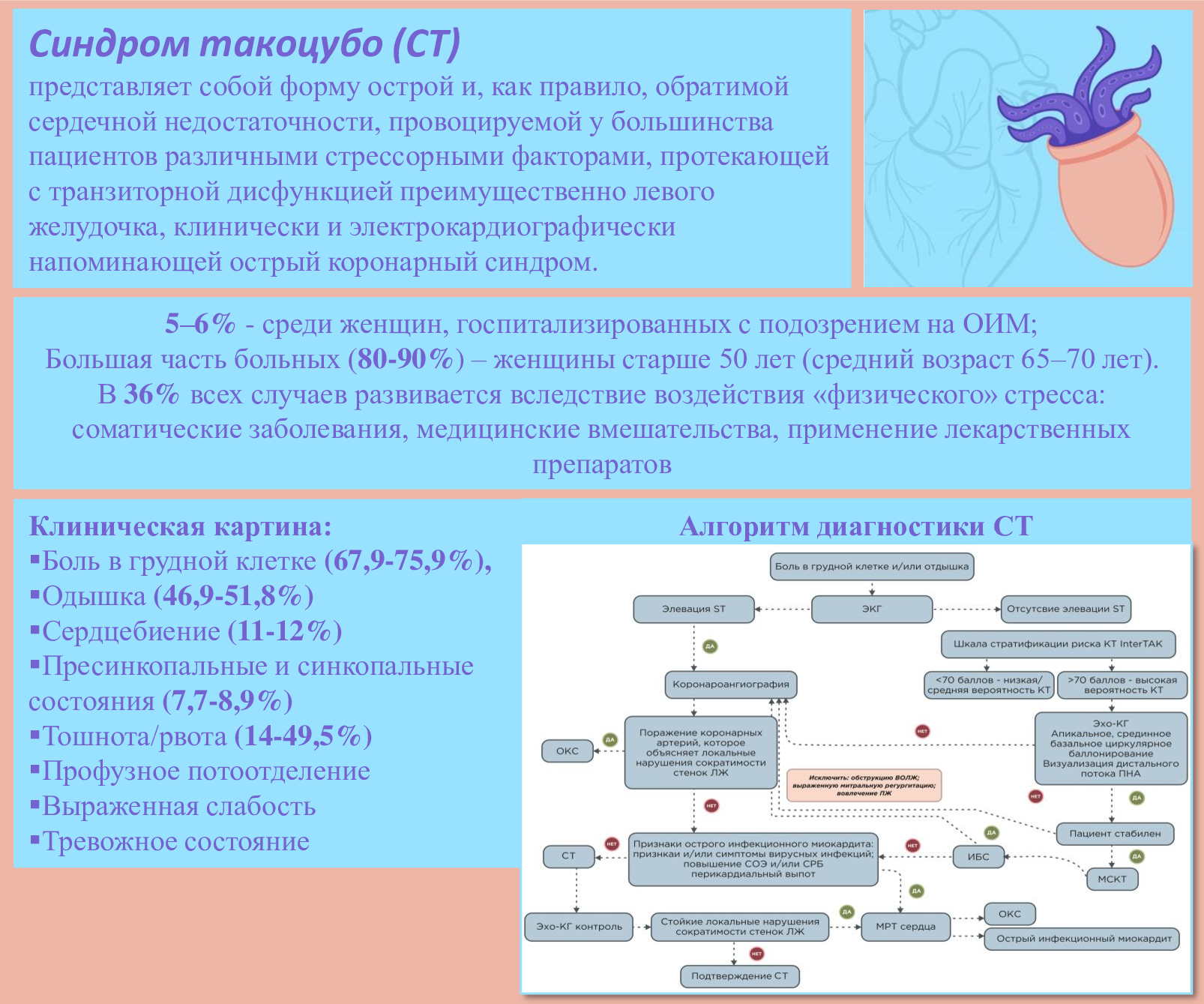
Синдром такоцубо (СТ) представляет собой острою обратимую дисфункцию миокарда левого желудочка, вызванную эмоциональным или физическим триггером. В периоперационном периоде СТ в некоторых случаях индуцируется различными психологическими факторами, такими как стресс до/после операции, и непсихологическими факторами, например — введение лекарственных препаратов. В данной статье приводится описание клинического наблюдения синдрома такоцубо, развившегося в раннем послеоперационном периоде ринопластики.
ISSN 2411-6564 (Online)